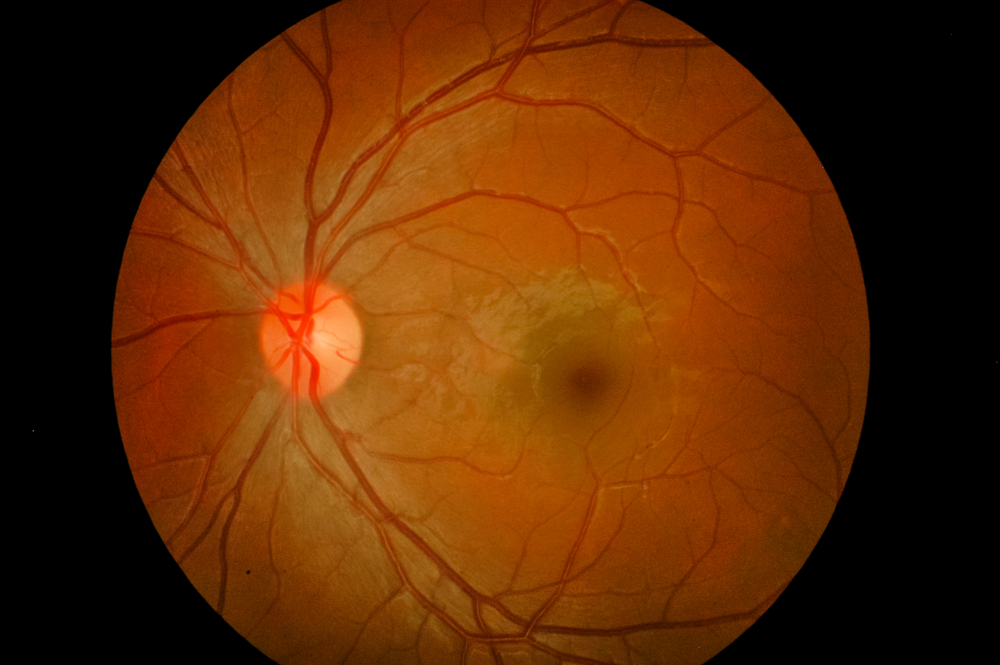
Die altersbedingte Makuladegeneration betrifft weltweit mehr als 200 Millionen Menschen. Dabei lässt sich zwischen trockener und feuchter AMD unterscheiden, wobei erstere Form den Großteil der Patienten ausmacht, während letztere als aggressiver gilt und zu schweren Sehbehinderungen führt. Ein frühes Symptom ist verschwommenes Sehen, bei dem gerade Linien verzerrt erscheinen. Dies kann zu Dunkelheit, Whiteouts oder verschwommenen Bereichen in der Mitte des Gesichtsfelds führen. AMD ist weltweit eine der Hauptursachen für irreversible Erblindung. Obwohl einige Therapien den Verlust des zentralen Sehvermögens verzögern, stellt keine aktuelle Behandlung ihn vollständig wieder her.
Abnormales Gefäßwachstum im Auge kann zu altersbedingter Makuladegeneration führen
Wissenschaftler der University of Virginia Health System haben ein neues Ziel identifiziert, um die Bildung abnormaler Verwicklungen von Blutgefäßen im Zusammenhang mit Augenerkrankungen wie neovaskulärer altersbedingter Makuladegeneration, proliferativer diabetischer Retinopathie und Ischämie zu verhindern.
Die Studie hat die Möglichkeit eröffnet, das anormale Wachstum von Blutgefäßen bei Augenkrankheiten zu mildern, indem sie auf die epigenetische Maschinerie abzielt. Durch lokales Targeting des epigenetischen Regulators haben die Forscher ein tieferes Verständnis dafür gewonnen, wie okulare Immunzellen einen Verlust der Kontrolle über das Wachstum von Blutgefäßen unter der Netzhaut verursachen können. Dieser Ansatz bietet auch eine neue Richtu Entwing für diecklung effektiverer, kostengünstigerer Interventionen, wodurch Probleme wie Arzneimittelresistenzen vermieden werden, die bei herkömmlichen Anti-VEGF-Therapien, die in klinischen Behandlungen eingesetzt werden, ein wachsendes Problem darstellen.
Wissenschaftler haben bereits gewusst, dass abnormales Gefäßwachstum im Auge durch übermäßige Mengen einer Substanz namens „vaskulärer endothelialer Wachstumsfaktor A“ oder VEGF, die eine wichtige Rolle bei der Bildung von Blutgefäßen spielt, angeheizt wird. Die neue Forschung identifiziert ein Schlüsselprotein, das den VEGF-Spiegel bestimmt. Die Blockierung dieses Proteins bei Labormäusen senkte deren VEGF-Spiegel signifikant und zwar gezielt, ohne unerwünschte Nebenwirkungen. Die Wissenschaftler stellten zum Beispiel fest, dass sie keine toxischen Wirkungen auf die Netzhaut hat, jenen lichtempfindlichen Teil des Auges, wo die Gefäßwucherung auftritt. Diese Entdeckung beantwortet eine seit langem bestehende Frage darüber, wie okulare Immunzellen wie Makrophagen zu einem abnormalen Wachstum von Blutgefäßen unter der Netzhaut beitragen.
Neben der Identifizierung eines vielversprechenden Ziels für die Entwicklung neuer Behandlungen gegen Sehverlust wirft die Entdeckung ein wichtiges Licht auf die grundlegenden Mechanismen, die für das Überwuchern von Blutgefäßen verantwortlich sind, das Millionen von Menschen das Augenlicht raubt. Während noch viel mehr Forschung und Tests erforderlich sein werden, bevor die neuen Erkenntnisse in eine Behandlung umgesetzt werden können, sind die Wissenschaftler vom Potenzial der Entdeckung begeistert.
Die Rolle von Immunzellen bei der Entstehung von
altersbedingter Makuladegeneration
Mit zunehmendem Alter altert auch das Immunsystem. Bereits zuvor haben Wissenschaftler der Washington University School of Medicine in St. Louis herausgefunden, dass alternde Immunzellen das Risiko für altersbedingte Makuladegeneration erhöhen, eine der Hauptursachen für Erblindung. Bei der Untersuchung von Mäusen und Zellen von Patienten stellten die Forscher fest, dass Immunzellen, Makrophagen genannt, altern und mit größerer Wahrscheinlichkeit zu Entzündungen und abnormalem Blutgefäßwachstum beitragen, die das Sehvermögen bei Makuladegeneration schädigen. Ihre Ergebnisse wurden in der Zeitschrift JCI Insight veröffentlicht.
In Experimenten an Mäusen fand das Team heraus, dass ältere Makrophagen größere Mengen an kurzen Schnipseln genetischen Materials, sogenannte microRNAs, tragen, die steuern, wie Zellen Gene exprimieren. Die Forscher fanden signifikant höhere Werte von microRNA-150 in Makrophagen in den Augen älterer Mäuse. MicroRNAs helfen, viele Dinge in Zellen zu regulieren, indem sie an mehrere Gene binden, um zu beeinflussen, wie diese Gene Proteine herstellen. In dieser Studie fanden die Forscher heraus, dass microRNA-150 in einem Mausmodell der Makuladegeneration anscheinend ältere Makrophagen dazu anleitet, Entzündungen und eine abnormale Bildung von Blutgefäßen zu fördern. Die Forscher testeten auch Blutproben von Menschen mit und ohne Makuladegeneration. Die Proben von Patienten mit Makuladegeneration hatten ebenfalls signifikant höhere Werte von microRNA-150 in ihren Makrophagen.
Makuladegenerationstherapien richten sich eher auf Krankheitssymptome als ihre Ursache zu behandeln. Durch das Verständnis, was mit den Immunzellen im Auge passiert, ist es vielleicht möglich, Therapien zu entwickeln, um Patienten zu helfen, denen mit bestehenden Medikamenten nicht geholfen werden kann. Wenn es gelingt, mikroRNA-Spiegel in Makrophagen irgendwie zu reduzieren oder einen oder mehrere molekulare Wege zu verändern, die von dieser mikroRNA reguliert werden, können möglicherweise Entzündungen gesenkt und das abnormale Wachstum von Blutgefäßen im Auge gestört werden.
Bestimmtes Protein spielt Schlüsselrolle bei vielen altersbedingten Krankheiten
Forschungen, die im Physical Journal veröffentlicht wurden, legen nahe, dass ein Schlüsselprotein im Blut an der Entstehung von Makuladegeneration und anderen altersbedingten Krankheiten wie Alzheimer und Atherosklerose beteiligt ist. Es gibt Hunderte von Proteinen in unserem Blut, aber die Forscher konzentrierten sich auf Vitronectin, eines der am häufigsten vorkommenden. Vitronektin zirkuliert nicht nur in hohen Konzentrationen im Blut, sondern auch im Gerüst zwischen den Zellen und ist auch ein wichtiger Bestandteil des Cholesterins. Dieses Protein ist ein wichtiger Angriffspunkt für die Makuladegeneration, weil es sich im Augenhintergrund ansammelt und zu Sehverlust führt. Ähnliche Ablagerungen treten im Gehirn bei der Alzheimer-Krankheit und in den Arterien bei Atherosklerose auf.
Durch detaillierte biochemische Analysen fanden die Forscher heraus, dass das Protein seine Form unter Druck subtil ändern kann. Diese Änderungen führen dazu, dass es sich leichter an Calciumionen im Blutbindet , was nach Ansicht der Forscher zur Bildung von verkalkten Plaqueablagerungen führt, die für Makuladegeneration und andere altersbedingte Erkrankungen charakteristisch sind. Diese strukturellen Erkenntnisse werden die Entwicklung von Behandlungen für Makuladegeneration rationalisieren, da sie es Forschern ermöglichen, Antikörper kundenspezifisch zu entwickeln, die selektiv die Kalziumbindung des Proteins blockieren, ohne seine anderen wichtigen Funktionen im Körper zu stören.
Übergewicht als Ursache für altersbedingte Makuladegeneration
Eine in der Zeitschrift Science veröffentlichte kanadische Studie deckt einen weiteren molekularen Mechanismus auf, der altersbedingte Makuladegeneration (AMD) auslösen kann. Die Forschung am Hôpital Maisonneuve-Rosement in Montreal zeigt, wie Lebensstressoren wie Fettleibigkeit die Zellen des Immunsystems umprogrammieren, und sie mit zunehmendem Alter für das Auge zerstörerisch machen.
Es ist bereits bekannt, dass das Immunsystem im Auge einer Person mit AMD dysreguliert und aggressiv wird. Normalerweise halten Immunzellen das Auge gesund, doch der Kontakt mit Krankheitserregern wie Bakterien und Viren kann sie schädigen. Gleichzeitig werden Immunzellen auch aktiviert, wenn der Körper Stressfaktoren ausgesetzt ist, wie zum Beispiel überschüssiges Fett bei Adipositas, was Übergewicht zum nicht-genetischen Risikofaktor Nummer eins für die Entwicklung von AMD macht.
In ihrer Studie verwendeten die Forscher Übergewicht als Modell, um die Stressoren zu beschleunigen und zu übertreiben, denen der Körper im Laufe des Lebens ausgesetzt ist. Sie fanden heraus, dass vorübergehende Fettleibigkeit oder eine Vorgeschichte von Fettleibigkeit zu anhaltenden Veränderungen in der DNA-Architektur innerhalb von Immunzellen führt, wodurch sie anfälliger für die Produktion von Entzündungsmolekülen werden. Diese Ergebnisse liefern wichtige Informationen über die Biologie der Immunzellen, die AMD verursachen, und könnten in Zukunft die Entwicklung maßgeschneiderterer Behandlungen ermöglichen.